下肢动脉硬化闭塞症
下肢动脉硬化闭塞症(Peripheral Arterial Disease,PDA)是动脉粥样化在下肢的重要肢体表现,可导致患者下肢缺血坏疽,甚至截肢等风险。随着社会的发展,人民生活水平的不断提高饮食结构改变,人口老龄化的进展,以及血管外科诊疗水平的不断发展,下肢动脉硬化闭塞症的发生率在中国呈增加趋势。
病因及危险因素
流行病学调查结果显示动脉粥样硬化与下列因素有关:高血压、高胆固醇、吸烟、肥胖、糖尿病、高甘油三脂血症、紧张、高同型半胱氨酸血症等。
机制和病理
机制:下肢动脉硬化闭塞症动脉粥样硬化的发病机理复杂,是多种因素长期综合性作用的过程。动脉壁内皮细胞受损、功能改变、渗透性增高,血液中的单核细胞粘附、侵润、进入内皮下,吞噬脂质成为泡沫细胞,形成脂肪斑,血小板聚集也在局部粘附、活化,吞噬细胞、内皮细胞及粘附于内皮细胞损伤处的血小板释放生长因子刺激平滑肌细胞进入内膜并增殖,脂肪斑变成纤维斑块,最终导致动脉粥样硬化下肢动脉硬化闭塞症。
累及部位:下肢动脉硬化闭塞症动脉粥样硬化主要累及下肢的大型弹力型动脉和中型肌弹力型动脉,包括髂,股,胭动脉均可受累,后期可延及其远端大的分支。糖尿病下肢动脉硬化闭塞的病变相对特殊,胫前、胫后和腓动脉受累多见,血管壁粥样硬化改变不明显。原因是下肢动脉粗长承受血液的压力大,动脉内膜受内外损伤的机会比较多。大腿内收肌管周围肌肉反复收缩机械性损伤有很大关系
下肢动脉粥样硬化的症状及体征
下肢动脉硬化闭塞症PDA早期的症状为间歇性跛行、远侧动脉搏动减弱或消失,下肢动脉硬化闭塞症后期可出现静息痛、皮肤温度明显降低、发绀、趾端溃疡、坏疽等。临床表现分为4期。第1期,轻微主诉期。患者仅感觉患肢皮温降低、怕冷,或轻度麻木,活动后易疲劳,肢端易发生足癣感染而不易控制。第2期,间歇性跛行期。当患者在行走时,由于缺血和缺氧,较常见的部位是小腿的肌肉产生痉挛、疼痛及疲乏无力,必须停止行走,休息片刻后,症状有所缓解,才能继续活动。如再行走一段距离后,症状又重复出现。小腿间歇性跛行是下肢缺血性病变最常见的症状。第3期,静息痛期。当病变进一步发展,而侧支循环建立严重不足,使患肢处于相当严重的缺血状态,即使在休息时也感到疼痛、麻木和感觉异常。疼痛一般以肢端为主。第4期,组织坏死期。主要指病变继续发展至闭塞期,侧支循环十分有限,出现营养障碍症状。在发生溃疡或坏疽以前,皮肤温度降低,色泽为暗紫色。早期坏疽和溃疡往往发生在足趾部,随着病变的进展,感染、坏疽可逐渐向上发展至足部、踝部、或者小腿,严重者可出现全身中毒症状。
实验室检查:
1.血脂检查 了解血总胆固醇、甘油三酯、β-脂蛋白、高密度脂蛋白以及低密度脂蛋白。
2.血糖、尿糖、血常规、同型半胱氨酸和血细胞比容测定 目的在于了解病人有无伴发糖尿病、贫血或红细胞增多症、以及是否存在高同型半胱氨酸。
3.ABI测压 通过下肢节段性测压及踝/肱指数测定可了解下肢缺血的部位和程度,目前已成为对下肢动脉闭塞病人的常规检查之一。大于1.下肢动脉正常,但大中动脉硬化弹性减退;下肢动脉硬化闭塞症0.9~1.1是正常;下肢动脉硬化闭塞症o.7-0.89是轻中度动脉度动脉硬化狭窄,临床上下肢动脉硬化闭塞症可伴有间歇性跛行或下肢动脉硬化闭塞症无任何症状,下肢动脉硬化闭塞症小于0.7提示中重度狭窄,下肢动脉硬化闭塞症患者多有间歇性跛行或静息痛。 下肢动脉硬化闭塞症如果ABI数值明显下降超过0.15,则表示下肢动脉硬化闭塞症动脉狭窄程度超过50%,如此程度的下肢动脉硬化闭塞症管腔狭窄常预示有可能会突然发生血栓堵塞。
4.超声检查 此属无损伤性血管检查,简易便行,可在术前、术后多次重复使用。目前是下肢动脉硬化闭塞症的重要筛选性检查。有利于观察斑块性质,了解血流特点及管腔狭窄程度,是否合并血栓。
5.下肢动脉CTA 能清晰客观的显示下肢动脉的解剖形态,侧枝建立情况,狭窄程度,但不能提供下肢动脉血流速度等信息。
6.下肢MRA MRA能显示周围动脉的解剖形态,但MRA所提供的图像以股动脉显像最佳,
7.下肢动脉DSA造影 ?目前是诊断下肢动脉硬化闭塞症的金标准。一般通过股动脉插入导管至腹主动脉注入造影剂,但如腹主动脉下端阻塞或两侧髂动脉阻塞者,可自上肢肱动脉插管至降主动脉做造影。因动脉造影具有一定危险性和并发症,且并非确诊本病所必需的方法,故不列为常规的检查步骤。
下肢动脉硬化闭塞症杂交技术
治下肢动脉硬化闭塞症杂交技术是指联合外科手术和腔内介入技术为一体优势互补的结合策略。术中血管造影并辅助腔内介入技术被认为是确保主要动脉及其分支的完全恢复灌注最可靠的方法。术中辅以腔内介入治疗来弥补外科手术治疗的不足使治疗更加完善。
2.1外科+腔内介入治疗
对急性动脉栓塞患者行切开动脉fogarty导管取栓(图1),选用不同型号导管顺行及逆行取栓,尽量将血栓取尽,使得出现良好喷血及回血,对合并动脉硬化斑块者术中行内膜剥脱及斑块切除(图2)。术中行动脉血管造影(图3),评估血管情况并观察有无未取尽血栓及其位置和局部解剖因素。有残余血栓时可行X线透视下超选择fogarty导管取栓(由于Fogarty导管头端无弯曲弧度,这样超选择动脉取栓要求术者有较高的操作技术及对血管解剖因素非常熟悉,具体的操作经验及实践尚需进一步积累,图4),和/或利用血栓吸引技术尽量将血栓取尽。利用超选择导丝导管技术造影远心端及近心端,必要时进行球囊扩张和/或支架植入(图5)。
Zaraca等证实取栓后术中常规行血管造影比选择性造影能发现更多的血管损害也就需要更多的腔内介入辅助治疗(即杂交治疗),这样预后也较好,24个月再狭窄的比率也较低[11]。术中血管造影不仅可以确定是否需要腔内介入辅助治疗且能指导其治疗,如血管成形及支架置入,这些处理措施能在取栓后立即进行也就简化并加快了治疗。
2.2外科+溶栓治疗
外科取栓术中合理的使用溶栓药物可使栓塞动脉的残余血栓连同移位的血栓以及取栓导管无法到达的分支血管里的血栓溶解。Norem等在切开动脉取栓术中动脉内灌注链激酶,结果附壁血栓能被取栓导管再次取栓时清除,最后造影显示有明显改善[12]。Parent等对术中造影发现取栓后腘动脉有残余血栓的患者动脉内灌注纤溶酶原激活物,延迟30 min后再次造影显示88%的患者达到血栓成功溶解[13]。
很多人担心术中动脉内灌注溶栓药物会增加出血的风险。事实上,采用动脉导管局部输注溶栓药物,很少会有纤溶酶原激活物或是纤溶酶进入循环系统,即使有限量进入循环系统也将迅速被循环中的拮抗剂中和,而不引起全身效应。一个多中心,随机,盲法和安慰剂对照实验研究,证实术中接受溶栓治疗是安全的,不增加出血相关并发症,并建议对肢体残余的顽固血栓及脱落栓子造成的多支血管急性栓塞使用超大剂量溶栓治疗,因为单剂量甚至双倍剂量的动脉内溶栓药物也是不够的,实验结果显示了术中接受尿激酶组的病人比接受安慰剂组的病人术后生存率高[14]。
溶栓治疗的选择依赖很多因素,例如病变的位置、解剖因素,闭塞持续时间,患者的风险因素(并存病)和操作过程相关的风险[15~17]。脱落至股部的栓子大多是在原始形成栓子器官已很长时间的陈旧性血栓,这种栓子没有在栓塞部位新近形成的血栓对溶栓酶敏感。溶栓相关禁忌症必须充分考虑。
2.3 溶栓+腔内介入治疗
现行溶栓导管溶栓治疗技术主要包括各种特异纤维蛋白溶解药物和多种局部输注方式(脉冲喷射,血栓内大剂量药物技术)。McNamara等认为治疗急性动脉栓塞最佳的方法是溶栓治疗,尤其是导丝能通过闭塞段成功置溶栓导管时治疗效果更好[18]。如果导丝不能通过闭塞段,中间可穿插一段时间的溶栓治疗,一段时间的溶栓治疗后导丝仍不能通过,可能预示着一个相对较差的治疗结果[19~20]。纵使成功置溶栓导管,溶栓过程中也应进行反复造影以明确血管走形及病变区域,若造影显示有潜在动脉局限性损害(动脉硬化狭窄或内膜损伤),尽管其很少引起急性动脉栓塞或是严重肢体缺血症状,但是这些因素可能会增加血栓形成,所以也应该处理。
机械血栓取除装置利用生理盐水喷雾连同文丘里效应在血栓局部持续搅拌(被认为是“水流的漩涡”),这样就有选择的捕捉,溶解和疏散血栓,取除效果主要取决于血栓的性质(新鲜的血栓比陈旧性血栓效果好),外部附加一个抽吸装置或高速旋转叶轮来取除血栓。转动的和液压的再循环装置可以缩短腔内治疗灌注溶栓药物时间,也就减少了出血相关并发症,但其使用经验尚有限且只限于小血管 [21~23]。经皮吸引血栓取除技术是用一个较大直径的导管连接一个负压针筒吸引血管内的血栓[24]。Wagner等利用经皮吸引血栓取除技术使86%的患者血管再通并获得灌注[25]。经皮吸引血栓取除技术是溶栓治疗的一个典型辅助应用,或是被用作外科未能完全除术的终末血栓的补救治疗。
机械血栓取除和经皮血栓取除技术可以提高动脉内溶栓的短期和长期疗效,帮助达到2种重要临床结果:联合溶栓用于移除不溶解的物质或是压实血栓来加快血流灌注的恢复,并且可以用于纠正溶栓过程或操作过程对血管造成的损害。

 联系我们
联系我们 地址:郑州市康复前街3号(郑州火车站西广场对面)。
地址:郑州市康复前街3号(郑州火车站西广场对面)。 乘车路线:乘坐40、夜班Y17、夜班Y2、G126、G81、201、70、256、58、729、217、20、981、213、176至火车站西广场(郑州大学第五附属医院)站下车。
乘车路线:乘坐40、夜班Y17、夜班Y2、G126、G81、201、70、256、58、729、217、20、981、213、176至火车站西广场(郑州大学第五附属医院)站下车。 地铁路线:乘坐地铁1号线至郑州火车站从C口出站。
地铁路线:乘坐地铁1号线至郑州火车站从C口出站。 急救电话:0371-6690 2126 / 6690 2120 (24小时)
急救电话:0371-6690 2126 / 6690 2120 (24小时)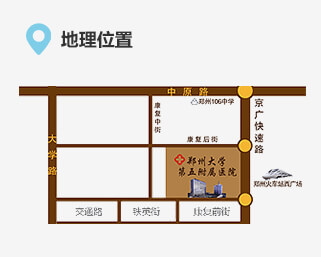 乘车路线:乘坐40、夜班Y17、夜班Y2、G126、G81、201、70、256、58、729、217、20、981、213、176至火车站西广场(郑州大学第五附属医院)站下车。地铁路线:乘坐地铁1号线至郑州火车站从C出口出站
乘车路线:乘坐40、夜班Y17、夜班Y2、G126、G81、201、70、256、58、729、217、20、981、213、176至火车站西广场(郑州大学第五附属医院)站下车。地铁路线:乘坐地铁1号线至郑州火车站从C出口出站







 李玉萍
李玉萍 杨楠
杨楠 田晓庚
田晓庚 宋俊莉
宋俊莉



 首页
首页




